Температуры кипения спиртов
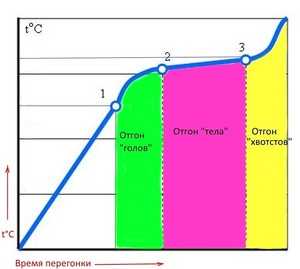 Чистый идеализированный спирт имеет градус кипения равный семидесяти восьми.
Чистый идеализированный спирт имеет градус кипения равный семидесяти восьми.
Как только брага нагревается до определённой температуры, первыми начинают испаряться самые летучие части. В первую очередь выпариваются метанол, уксусный альдегид и прочие особо опасные яды. Это происходит уже при температуре кипения 64–67 градусов.
Второй этап – отделяется этиловый спирт – огонь нагрева убавляют до минимального. Таким образом, поддерживается температура около 62–64 градусов. Именно эту температуру необходимо поддерживать на протяжении всей перегонки. Однако, температура перегонки самогона в ёмкости постепенно растёт по мере испарения спирта.
Когда температура поднимается до 85 градусов, начинается третий этап. Сейчас весь возможный этиловый спирт уже отделился, и за ним выпариваются сивушные масла. Это тоже ядовитые вещества, которые не употребляют для питьевых целей.
Нельзя допустить поднятия температуры до 95 градусов и выше. Такой перегрев приведёт к выбросу браги в остужающий элемент самогонного аппарата. Это заметно ухудшит качество конечного напитка, его цвет и вкус.
Важные моменты
Некоторые винокуры утверждают, что «хвостики» можно перегнать, добавив их к новой бражке. Магистры зелий не соглашаются и приводят весьма обоснованные доводы. В последней части содержится ничуть не меньше примесей и сивушных масел, чем и в первой. Повторный перегон с новой брагой подпортит вкус добываемого эликсира и прибавит мутноватого оттенка.
Выгонка забористых спиртных нектаров дома – не сложный алхимический процесс. Но ведь каждому любитлю-экспериментатору хочется получить шедевр, а не суррогат. Мастерами зелий веками нарабатывался опыт путем множества проб и ошибок. Используя проверенные методы и соблюдая температурные правила, Вам удастся дистиллировать настоящий эликсир. А игнорирование рекомендаций и спешка – главный враг в этом деле.
- Ошибки могут привести не только к снижению качества напитка, но навредить здоровью дегустатора.
- Чрезмерное увеличение температуры, навредит букету и цвету самогона, а выдерживание правильного градуса позволит ощутить триумф победы.
Теперь, вооружившись вышеуказанными памятками, вы сможете грамотно провести весь процесс самогоноварения и порадовать себя и друзей бутылочкой достойного вида и качества напитка.
Посмотрите видео, в котором рассказывается о температуре отделения головных фракций:
Конечный продукт
На выходе, может получиться практически какой угодно напиток. Дело вкусов и фантазии. Критериев для оценки конечного продукта немного:
- Вкус.
- Степень очистки.
- Рецептура (для ценителей).
 Когда стало, наконец, ясно, как правильно выгнать самогон из браги, можно приступать к экспериментам. Вариантов конечного продукта великое множество и нет никаких ограничений по вкусам и рецептуре, было бы желание! Потому самогоноварение и называют целым искусством создания крепких напитков.
Когда стало, наконец, ясно, как правильно выгнать самогон из браги, можно приступать к экспериментам. Вариантов конечного продукта великое множество и нет никаких ограничений по вкусам и рецептуре, было бы желание! Потому самогоноварение и называют целым искусством создания крепких напитков.
Сколько требуется времени, сил и средств мастерам для получения качественного продукта, доподлинно известно быть просто не может. Процесс создания из браги хорошего самогона отнимает много сил и времени и становится для многих настоящим хобби.
Свойства испарения
Экспериментально установлены следующие cвойства испарения:
- При одинаковых условиях различные вещества испаряются с различной скоростью (скорость испарения определяется числом молекул, переходящих в пар с поверхности вещества за 1 с).
- Скорость испарения тем больше:
- чем больше площадь свободной поверхности жидкости;
- чем меньше плотность паров над поверхностью жидкости. Скорость увеличивается при движении окружающего воздуха (ветер);
- чем больше температура жидкости.
- При испарении температура тела понижается.
Механизм испарения можно объяснить с точки зрения MKT: молекулы, находящиеся на поверхности, удерживаются силами притяжения со стороны других молекул вещества. Молекула может вылететь за пределы жидкости лишь тогда, когда ее кинетическая энергия превышает значение той работы, которую необходимо совершить, чтобы преодолеть силы молекулярного притяжения (работа выхода). Поэтому покинуть вещество могут только быстрые молекулы. В результате средняя кинетическая энергия оставшихся молекул уменьшается, а температура жидкости понижается. Для того, чтобы поддерживать температуры испаряющейся жидкости неизменной, к ней необходимо подводить некоторое количество теплоты.
Молекулы пара хаотически движутся. Поэтому некоторые из них могут снова возвратиться в жидкость. Процесс перехода вещества из газообразного состояния в жидкое называется конденсацией.
Число возвратившихся в жидкость за определенный промежуток времени молекул тем больше, чем больше концентрация молекул пара, а следовательно, чем больше давление пара над жидкостью. Конденсация пара сопровождается нагреванием жидкости. При конденсации выделяется такое же количество теплоты, которое было затрачено при испарении.
Кипение жидкостей
Кипение — это парообразование, происходящее одновременно и с поверхности, и по всему объему жидкости. Оно состоит в том, что всплывают и лопаются многочисленные пузырьки, вызывая характерное бурление.
Как показывает опыт, кипение жидкости при заданном внешнем давлении начинается при вполне определенной и не изменяющейся в процессе кипения температуре и может происходить только при подводе энергии извне в результате теплообмена (рис. 3):
\(~Q = L \cdot m,\)
где L — удельная теплота парообразования при температуре кипения.
Рис. 3
Механизм кипения: в жидкости всегда имеется растворенный газ, степень растворения которого понижается с ростом температуры. Кроме того, на стенках сосуда имеется адсорбированный газ. При нагревании жидкости снизу (рис. 4) газ начинает выделяться в виде пузырьков у стенок сосуда. В эти пузырьки происходит испарение жидкости. Поэтому в них, кроме воздуха, находится насыщенный пар, давление которого с ростом температуры быстро увеличивается, и пузырьки растут в объеме, а следовательно, увеличиваются действующие на них силы Архимеда. Когда выталкивающая сила станет больше силы тяжести пузырька, он начинает всплывать. Но пока жидкость не будет равномерно прогрета, по мере всплытия объем пузырька уменьшается (давление насыщенного пара уменьшается с понижением температуры) и, не достигнув свободной поверхности, пузырьки исчезают (захлопываются) (рис. 4, а), вот почему мы слышим характерный шум перед закипанием. Когда температура жидкости выравняется, объем пузырька при подъеме будет возрастать, так как давление насыщенного пара не изменяется, а внешнее давление на пузырек, представляющее собой сумму гидростатического давления жидкости, находящейся над пузырьком, и атмосферного, уменьшается. Пузырек достигает свободной поверхности жидкости, лопается, и насыщенный пар выходит наружу (рис. 4, б) — жидкость закипает. Давление насыщенного пара при этом в пузырьках практически равно внешнему давлению.
Рис. 4
Температура, при которой давление насыщенного пара жидкости равно внешнему давлению на ее свободную поверхность, называется температурой кипения жидкости.
Так как давление насыщенного пара увеличивается с ростом температуры, а при кипении оно должно быть равно внешнему, то при увеличении внешнего давления температура кипения увеличивается.
Температура кипения зависит также от наличия примесей, обычно увеличиваясь с ростом концентрации примесей.
Если предварительно освободить жидкость от растворенного в ней газа, то ее можно перегреть, т.е. нагреть выше температуры кипения. Это неустойчивое состояние жидкости. Достаточно небольших сотрясений и жидкость закипает, а ее температура сразу понижается до температуры кипения.
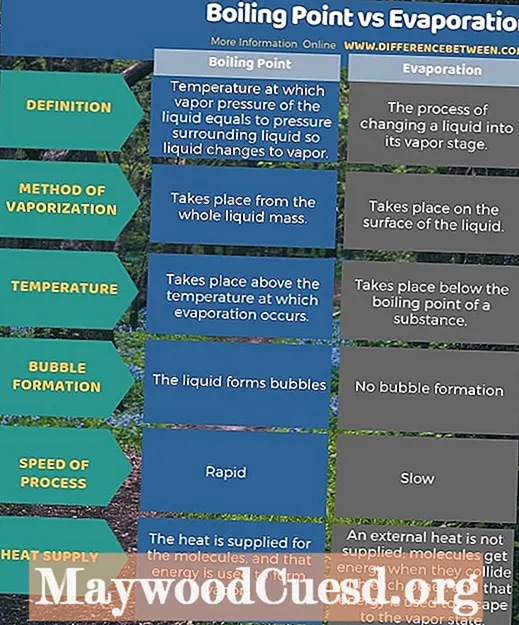
В чем разница между температурой кипения и испарением?
Точка кипения вещества — это температура, при которой давление пара жидкости равно давлению, окружающему жидкость, и жидкость превращается в пар. В то время как испарение — это процесс превращения жидкости в паровую стадию. Следовательно, ключевое различие между точкой кипения и испарением заключается в том, что испарение происходит на поверхности жидкости, тогда как при температуре кипения испарение происходит из всей массы жидкости. Здесь испарение конкретной жидкости происходит ниже точки кипения.
Кроме того, при температуре кипения жидкость образует пузырьки, и при испарении пузырьки не образуются. Следовательно, это заметная разница между температурой кипения и испарением.Кроме того, при температуре кипения молекулам передается тепло, и эта энергия используется для образования паров. Но при испарении внешнее тепло не подводится. Скорее, молекулы получают энергию, когда они сталкиваются друг с другом, и эта энергия используется для перехода в парообразное состояние. Следовательно, это значительная разница между температурой кипения и испарением.
Ниже приведена инфографика о разнице между температурой кипения и испарением, в которой перечислены все эти различия.
В чем разница между процессами?
Есть отличия между этими двумя процессами. Если испарение — это парообразование, происходящее при комнатной температуре, то кипением называют преобразование воды в пар при достижении температуры кипения. Эта температура будет постоянной на протяжении всего процесса кипения.
При парообразовании, происходящем на поверхности воды, расположенные там молекулы участвуют в этой процедуре наибольшую часть времени.
Основное отличие этих процессов состоит в том, что для кипения свойственно поддержание постоянной температуры, в результате чего происходит газообразование, а испарение — это спонтанный, а не принудительный процесс, поддерживаемый изменением давления или температуры.
Кипение считают массовым явлением, происходящим во всём теле жидкости, в то время как, испарение затрагивает исключительно поверхностные молекулы. Кипячение приводит к образованию пузырьков во внутренней структуре, откуда они поднимаются и преобразуются в газ.
Практическое применение процесса испарения спирта
Процесс испарения спирта имеет широкое практическое применение в различных областях:
- Медицина: испарение спирта используется для обработки ран, инструментов и поверхностей, так как спирт обладает антисептическими свойствами.
- Парфюмерия и косметика: при производстве духов и лосьонов спирт используется как растворитель для ароматических веществ.
- Алкогольная промышленность: процесс испарения спирта является основой для производства различных спиртных напитков, таких как водка, ром, виски и другие.
- Промышленность: спирт используется в процессах экстракции, сублимации и как растворитель для различных веществ в производстве лакокрасочных материалов, растворителей, парфюмерии и многих других промышленных продуктов.
Также процесс испарения спирта играет значительную роль в химических реакциях, в процессе дистилляции, сушки, выделения и очистки веществ.
Теоретические аспекты
Температура кипения и летучесть примесей
Самое распространенное заблуждение среди начинающих самогонщиков гласит, что примеси испаряются пропорционально своей температуре кипения. На самом деле это в корне не так: летучесть примесей, то есть их способность покидать кипящую жидкость, никак не связана с температурами кипения этих примесей.
Рассмотрим классический пример о метаноле и изоамилоле. Пусть в куб залито сырье следующего состава (см. таблицу).
| Состав перегоняемой жидкости | Температура кипения веществ (°C) | Соотношение в растворе (%) |
| вода | 100 | 86 |
| этиловый спирт | 78 | 12 |
| метанол | 65 | 1 |
| изоамилол | 132 | 1 |
Доведем смесь до кипения (температура в кубе около 92 °C) и отберем небольшое количество дистиллята так, чтобы состав кипящего сырья практически не изменился. Каким будет состав отобранного дистиллята? Для воды и этилового спирта изменение концентраций можно легко найти по кривой равновесия или таблицам: концентрация спирта возрастет с 12 до 59%.
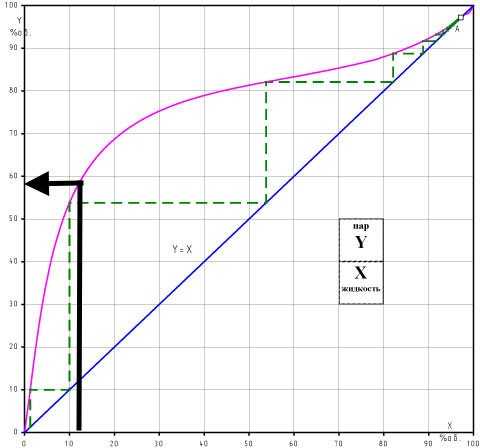 Кривая равновесия воды и этилового спирта
Кривая равновесия воды и этилового спирта
Чтобы определить изменение концентрации примесей, воспользуемся графиком коэффициентов ректификации (крепость в процентах от объема – на верхней горизонтальной оси).
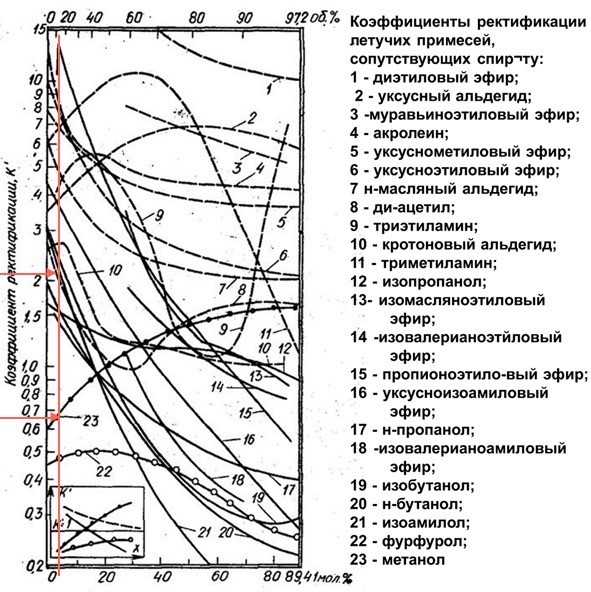
При крепости сырья 12% коэффициент ректификации (Кр) метилового спирта равен 0,67, а Кр изоамилола – 2,1. Значит, содержание метанола в отборе уменьшится, а изоамилола – возрастет в два раза. В результате получается.
| Состав перегоняемой жидкости | Температура кипения веществ (°C) | Соотношение в растворе (%) | Изменение количества | |
| в сырье | в дистилляте | |||
| вода | 100 | 86 | 38.2 | меньше в 2,2 раза |
| этиловый спирт | 78 | 12 | 59 | больше в 4,9 раза |
| метанол | 65 | 1 | 0.67 | меньше в 1,5 раза |
| изоамилол | 132 | 1 | 2.1 | больше в 2,1 раза |
Вторая таблица доказывает независимость скорости испарения примесей от температуры их кипения. Метанол с температурой кипения 65 °C медленнее покидает куб, чем изоамилол с температурой кипения 132 градуса.
Это происходит потому что концентрация этих примесей мала. Если бы количество метанола и изоамилола было сопоставимо со спиртом и водой, эти вещества заявили бы о своем праве на испарение в количестве, соответствующем разнице их температур кипения, и стали бы полноправными составляющими раствора.
Так и с примесями. Когда в растворе одну маленькую молекулу метанола окружает толпа молекул воды, то они легко удерживают её рядом с собой. Поскольку молекула метанола меньше этанола, то воде удерживать её намного легче. А вот изоамилол, наоборот, плохо растворяется в воде, имея с ней очень слабые связи. При кипении изоамилол вылетает из воды быстрее метанола, хотя температура его кипения в 2 раза выше.
Исследованию коэффициентов испарения или летучести различных веществ и их растворов посвятил немало своих трудов Сорель. Он составил таблицы и графики, по которым можно узнать, насколько меняется содержание веществ в парах по отношению к исходному раствору. Однако для целей винокурения графиками и таблицами пользоваться неудобно, поэтому Барбе предложил новый расчетный коэффициент, названный коэффициентом ректификации (Кр), для получения которого нужно при заданной крепости раствора разделить коэффициент испарения примеси на коэффициент испарения этилового спирта.
Коэффициент ректификации одновременно является и коэффициентом очистки, так как показывает фактическое изменение содержания примесей по отношению к этиловому спирту:
- Кр=1 – от примесей нельзя избавиться, они в том же количестве будут присутствовать в дистилляте;
- Кр>1 – в отборе примесей будет больше, чем в исходном сырье, это головные фракции;
- Кр 1 – это промежуточные примеси. Таких абсолютное большинство. Есть еще и концевые примеси, у которых, наоборот, Кр>1 при высокой концентрации спирта, а при низкой – Кр 1 —головные; 2 — промежуточные; 3 —хвостовые; 4 — концевые.
Головные примеси по мере продвижения вверх по колонне попадают во все более укрепленный пар, в результате их Кр возрастает. Это позволяет головным примесям с ускорением попадать в зону отбора.
Хвостовые примеси – строго наоборот, попав в колонну, с каждой новой теоретической тарелкой резко уменьшают свой Кр и довольно быстро вместе с флегмой оказываются внизу колонны, где и накапливаются.
Концевые примеси ведут себя похоже: при низкой крепости их Кр (283)
Что такое кипение?
Кипение происходит при определенной температуре, называемой точкой кипения. Точка кипения зависит от давления, поэтому при увеличении давления точка кипения также повышается. Обратно, при снижении давления точка кипения уменьшается.
Когда жидкость начинает кипеть, ее молекулы приобретают достаточную энергию, чтобы преодолеть силы притяжения друг к другу и перейти в газообразное состояние. При кипении происходит интенсивное образование пузырьков пара, которые возникают на разных глубинах жидкости и перемещаются к поверхности.
Кипение является важным процессом для различных приложений. Например, в процессе приготовления пищи мы используем кипение для варки воды или приготовления различных жидких продуктов. Кипение также широко используется в промышленности, научных исследованиях и многих других областях.
Определение и процесс кипения
Отличие между кипением и испарением заключается в процессе превращения жидкости в пар. В случае испарения, это происходит с поверхности жидкости при любой температуре, но при кипении процесс происходит внутри жидкости и требует достижения определенной температуры, которая зависит от внешних условий, включая давление.
Когда жидкость нагревается, ее частицы приобретают большую кинетическую энергию. При достижении точки кипения энергия частиц становится достаточно высокой, чтобы преодолеть межмолекулярные силы и выйти из жидкостной фазы в виде пара.
Во время кипения происходит интенсивное образование пара, образуется огромное количество пузырьков. Когда пузырьки достигают поверхности жидкости, они лопаются и пар выходит в окружающую среду.
Температура, при которой происходит кипение, зависит от давления. Например, вода кипит при 100°C при нормальном атмосферном давлении, но при сниженном давлении (на высоте) точка кипения воды уменьшается.
Итак, кипение — это процесс фазового перехода жидкости в пар при достижении определенной температуры и зависит от давления.
Температура и давление при кипении
Температура, при которой происходит кипение, зависит от давления. Обычно называется стандартная температура кипения, и для воды она равна 100 °C при атмосферном давлении. Однако, под действием высокого давления, температура кипения может быть значительно выше.
Отличие между кипением и испарением в том, что при кипении происходит фазовый переход на всей поверхности жидкости, в то время как при испарении молекулы жидкости переходят в газовую фазу только с поверхности жидкости.
Давление также влияет на скорость испарения и кипения. При повышенном давлении более высокая температура требуется для кипения, так как давление поддерживает жидкость в жидком состоянии и препятствует фазовому переходу.
Таким образом, температура и давление играют важную роль в процессах кипения и испарения, и их взаимодействие определяет условия, при которых происходят эти фазовые переходы.
Примеры практического применения кипения
Одним из примеров практического применения кипения является использование этого процесса в котлах для отопления и горячего водоснабжения. При нагревании воды в котле происходит ее кипение. Пар, образующийся в результате кипения, распространяется по системе трубопроводов, обеспечивая тепло в помещениях и горячую воду в кранах.
Еще одним примером применения кипения является работа паровых турбин. При нагреве водяного пара в специальных паровых котлах происходит его кипение. Образованный пар используется для привода турбины, которая в свою очередь приводит в движение генератор электричества.
Кипение также широко используется в пищевой промышленности при приготовлении пищевых продуктов. Например, при кипячении воды для приготовления макарон или картофеля. Также, при приготовлении пищевого жира происходит его расплавление и последующее кипение.
В области медицины кипение может использоваться для стерилизации медицинского оборудования. Высокая температура пара, образующегося при кипении, помогает уничтожить бактерии и микроорганизмы, делая инструменты безопасными для использования.
Таким образом, кипение находит широкое применение в различных сферах жизни, обеспечивая нам тепло, электричество, приготовленную пищу и безопасность.
Скорость испарения спирта: факторы, влияющие на процесс
Один из основных факторов, влияющих на скорость испарения спирта, — это температура окружающей среды. Чем выше температура, тем быстрее происходит испарение спирта. При повышении температуры молекулы спирта получают больше энергии, что способствует их более активному движению и, следовательно, более быстрому испарению.
Также важным фактором является площадь поверхности жидкости. Чем больше площадь поверхности спирта, тем больше молекул спирта находится на границе раздела с воздухом. Благодаря этому, молекулы легче покидают жидкость и переходят в газообразное состояние.
Важное влияние на процесс испарения спирта оказывает также наличие примесей в жидкости. Наличие других веществ может как ускорить, так и замедлить скорость испарения спирта
Некоторые вещества, такие как сахар, соль или другие спирты, могут образовывать силные межмолекулярные взаимодействия с молекулами спирта, что затрудняет их испарение.
Фактор влажности воздуха также может влиять на скорость испарения спирта. При высокой влажности испарение спирта замедляется, поскольку воздух уже содержит большое количество водяных паров, а спирт не может эффективно испаряться в насыщенной воздухом среде.
Для измерения скорости испарения спирта используются различные методы, включая гравиметрический анализ, хроматографию и газовую хроматографию. Гравиметрический анализ основан на измерении изменения массы жидкости при ее испарении. Хроматографические методы позволяют определить количество испарившегося спирта и его состав.
| Фактор | Влияние |
|---|---|
| Температура | Чем выше температура, тем быстрее испарение |
| Площадь поверхности | Чем больше площадь поверхности, тем быстрее испарение |
| Примеси | Могут как ускорить, так и замедлить испарение |
| Влажность воздуха | Высокая влажность может замедлить испарение |
Вода — растворитель
Вода является хорошим растворителем. Растворами называют однородные системы, состоящие из молекул растворителя и частиц растворенного вещества, между которыми происходят физические и химические взаимодействия. Например: механическое перемешивание — это физическое явление, нагревание при растворении серной кислоты в воде — химическое явление.
Суспензии — это взвеси, в которых мелкие частицы твердого вещества равномерно распределены между молекулами воды. Например: смесь глины с водой.
Эмульсии — это взвеси, в которых мелкие капельки какой-либо жидкости равномерно распределены между молекулами другой жидкости. Например: взбалтывание керосина, бензина и растительного масла с водой.
Раствор, в котором данное вещество при данной температуре больше не растворяется, называется насыщенным, а раствор, в котором вещество еще может растворяться, — ненасыщенным.
Растворимость определяется массой вещества, массой вещества, способной растворяться в 1000мл растворителя при данной температуре.
Массовая доля растворенного вещества — это отношение массы растворенного вещества к массе раствора.
Все знают, что если развесить выстиранное белье, то оно высохнет. И так же очевидно, что мокрый тротуар после дождя обязательно станет сухим.
Испарение — это процесс, при котором жидкость постепенно переходит в воздух в форме пара или газа. Все жидкости испаряются с разной скоростью. Спирт, аммиак и керосин испаряются быстрей воды.
Есть две силы, воздействующие на молекулы, из которых состоят все вещества. Первая — это сцепление, которое удерживает их между собой. Другая — тепловое движение молекул, которое заставляет их разлетаться в разные стороны. Когда эти две силы уравновешены, мы имеем жидкость.
На поверхности жидкости ее молекулы находятся в движении. Эти молекулы, которые движутся быстрей соседних, находящихся внизу, могут улетать в воздух, преодолевая силы сцепления. Это и является испарением.
Когда жидкость подогрета, испарение происходит быстрей. Так происходит потому, что в теплой жидкости скорость движения молекул больше, больше молекул имеет шанс покинуть жидкость. В закрытом сосуде испарение отсутствует. Так случается потому, что количество молекул в паре достигает определенного уровня. Тогда количество молекул, покидающих жидкость, будет равно количеству молекул, вернувшихся в нее. Когда это происходит, мы можем сказать, что пар достиг точки насыщения.
Когда воздух над жидкостью движется, скорость испарения увеличивается. Чем больше поверхность испаряющейся жидкости, тем быстрее происходит испарение. Вода в круглой сковородке испарится быстрей, чем в высоком кувшине.
Куда исчезает вода, когда она высыхает?
Выглянув на улицу или посмотрев на дорогу, вы увидели там воду. Один час яркого солнечного света — и вода исчезает! Или, например, вывешенное на веревке белье высыхает к концу дня. Куда исчезает вода?
Мы говорим, что вода испаряется. Но что это значит? Испарение — это процесс, при котором жидкость на воздухе быстро становится газом или паром. Многие жидкости испаряются очень быстро, гораздо быстрее, чем вода. Это относится к алкоголю, бензину, нашатырному спирту. Некоторые жидкости, например ртуть, испаряются очень медленно.
Из-за чего происходит испарение? Чтобы понять это, надо кое-что представлять о природе материи. Насколько мы знаем, каждое вещество состоит из молекул. Две силы оказывают воздействие на эти молекулы. Одна из них — сцепление, которое притягивает их друг к другу. Другая — это тепловое движение отдельных молекул, которое заставляет их разлетаться.
Если сила сцепления выше, вещество остается в твердом состоянии. Если же тепловое движение настолько сильно, что оно превосходит сцепление, то вещество становится или является газом. Если две силы примерло уравновешены, то тогда мы имеем жидкость.
Вода, конечно, является жидкостью. Но на поверхности жидкости есть молекулы, которые движутся настолько быстро, что преодолевают силу сцепления и улетают в пространство. Процесс вылета молекул и называется испарением.
Почему вода испаряется быстрее, когда она находится на солнце или нагревается? Чем выше температура, тем интенсивнее тепловое движение в жидкости. Это значит, что все большее количество молекул набирает достаточную скорость, чтобы улететь. Когда улетают самые быстрые молекулы, скорость оставшихся молекул в среднем замедляется. Почему остающаяся жидкость охлаждается за счет испарения.
Так что, когда вода высыхает, это означает, что она превратилась в газ или пар и стала частью воздуха.
Итоги
В данной статье мы рассмотрели основные принципы и различия между кипением и испарением.
- Кипение — это процесс перехода жидкости в газообразное состояние при достижении определенной температуры и давления. Испарение — это процесс перехода молекул жидкости в газообразное состояние без нагревания жидкости до точки кипения.
- Кипение происходит на всей поверхности жидкости, тогда как испарение происходит только на поверхности жидкости.
- Для кипения необходимо достичь определенной температуры и давления, которые зависят от вида жидкости и внешних условий. Для испарения достаточно, чтобы молекулы жидкости приобрели энергию, достаточную для преодоления сил притяжения между ними.
- В процессе кипения температура жидкости остается постоянной до тех пор, пока вся жидкость не превратится в пар. В процессе испарения температура жидкости понижается, так как в процессе испарения у частей молекул отнимается энергия для преодоления сил притяжения.
- Кипение обычно происходит при более высоких температурах, чем испарение. Кипящую жидкость можно видеть в виде пузырьков, образующихся на поверхности. При испарении жидкость остается спокойной и видимого пузырька нет.
Надеемся, что данная информация помогла вам понять разницу между кипением и испарением, а также принципы, по которым эти процессы происходят.




























